PRB 01-4F
OZONE : L'ÉCRAN SOLAIRE DE LA TERRE
Rédaction
:
Joanne Agterberg, Daniel Brassard
Division des sciences et de la technologie
Le 2 avril 2001
TABLE DES MATIÈRES
A. Équilibre du rayonnement thermique
1. Incidence sur la santé humaine
2. Incidence sur la flore terrestre
3. Incidence sur la vie aquatique
4. Incidence sur la pollution atmosphérique
SUBSTANCES DESTRUCTRICES DE L’OZONE
MESURES VISANT LA RÉDUCTION DES AGENTS DESTRUCTEURS
B. Initiatives du gouvernement fédéral
C. Mesures fédérales-provinciales
D. Mesures qui restent à prendre
ANNEXE : Substances destructrices de l’ozone
OZONE : L’ÉCRAN SOLAIRE DE LA TERRE
INTRODUCTION
La vie sur Terre repose sur un équilibre délicat entre de nombreux éléments différents. Les conditions nécessaires à la diversité et à l’abondance des formes de vie sont assez restrictives, et un changement majeur peut avoir des résultats imprévisibles. C’est l’énergie du soleil qui permet la vie, sous toutes ses formes, sur la planète bleue.
Le rayonnement ultraviolet (UV) est l’une des principales composantes de l’énergie solaire transmise à la Terre. Ce rayonnement, nécessaire en quantités modérées, peut, en quantités excessives, entraîner de graves problèmes pour l’homme et pour la biosphère en général. L’ozone présent dans la stratosphère atténue la quantité de rayonnement qui atteint la surface de la Terre. La stratosphère est une couche de l’atmosphère située en altitude, caractérisée par une inversion thermique, et où l’ozone joue pour la Terre un rôle d’écran solaire en filtrant les longueurs d’onde UV les plus dangereuses.
Depuis les années 1970, nous savons que diverses substances de synthèse détruisent cette couche protectrice. Les résultats d’études menées par la National Aeronautics & Space Administration (NASA) des États-Unis suggèrent que la perte d’ozone dans la haute atmosphère du Nord continuera d’augmenter dans les années à venir(1). Selon plusieurs modèles scientifiques et un rapport publié par Environnement Canada, les épisodes d’appauvrissement grave pourraient devenir plus fréquents au cours des 20 prochaines années, et ce serait entre 2010 et 2020 que les cas de destruction seraient les plus fréquents dans l’Arctique(2). Le présent document examinera les divers aspects du problème de l’ozone, depuis ses causes techniques jusqu’aux plus récents efforts faits pour le régler.
Au fil des temps géologiques, l’atmosphère a connu des changements et est devenue cette couche protectrice de la Terre qui permet la présence de la vie. La vie sur Terre a évolué lentement, de sorte que chaque élément de l’écosystème s’est adapté pour tirer le meilleur parti des conditions existantes. Au cours du dernier siècle, l’activité humaine a modifié l’atmosphère à une vitesse qui défie la nature et a ainsi réduit la capacité d’adaptation de certains organismes.
Certaines modifications de notre environnement sont évidentes; d’autres, plus difficiles à déceler. Le smog, par exemple, se remarque facilement; par contre, la modification des propriétés d’absorption et de réflexion de l’atmosphère est plus difficile à constater directement.
Il faut posséder une connaissance de base des processus qui interviennent dans ce phénomène pour apprécier pleinement l’importance de la baisse de la quantité d’ozone dans la haute atmosphère. L’ozone (O3) est un gaz légèrement bleuté, d’odeur piquante, comportant un atome d’oxygène de plus que l’oxygène moléculaire (O2). Il est présent au niveau du sol sous la forme de pollution, et y est dangereux pour la vie; il est aussi naturellement présent dans l’atmosphère jusqu’à une altitude d’environ 60 km (figure 1). En règle générale, 85 p. 100 de tout l’ozone se situe dans une région de la stratosphère, d’altitude variable selon la latitude, connue sous le nom de « couche d’ozone »(3). En moyenne, la quantité totale d’ozone présente dans la stratosphère est de 300 dobsons, ce qui équivaut à une épaisseur d’ozone pur de seulement 3 mm, à la pression au niveau du sol et à 0 °C. Lorsque l’ozone stratosphérique tombe à moins de 200 dobsons, on considère que c’est le début d’un « trou » d’ozone.
Figure 1

Profil vertical typique de la densité d’ozone aux latitudes moyennes de l’hémisphère Nord (unités = dobsons/kilomètre). La stratosphère se situe entre la tropopause et la stratopause. En superposition figurent des tracés du rayonnement UV en fonction de l’altitude pour les UV-A (320 à 400 nm), les UV-B (280 à 320 nm) et les UV-C (200 à 280 nm). La largeur de la barre représente la quantité d’énergie en fonction de l’altitude. L’énergie des UV-C baisse spectaculairement avec l’augmentation de l’ozone, à cause de la forte absorption dans la plage de longueurs d’onde de 200 à 280 nm. Les UV-B sont aussi beaucoup absorbés, et seule une petite fraction en atteint la surface. Les UV-A ne sont que faiblement absorbés par l’ozone, avec une certaine diffusion près de la surface(4).
L’ozone se forme lorsque du rayonnement de haute énergie, comme le rayonnement ultraviolet, dissocie les molécules d’oxygène en deux atomes d’oxygène qui se recombinent avec d’autres molécules d’oxygène. La concentration stratosphérique d’ozone atteint de nouveaux points d’équilibre selon les vitesses relatives de sa formation et de sa destruction, qui elles-mêmes dépendent de plusieurs conditions. Les pertes maximales d’ozone surviennent aux altitudes où il est le plus abondant, comme le montre la figure 2(5).
Figure 2(6)
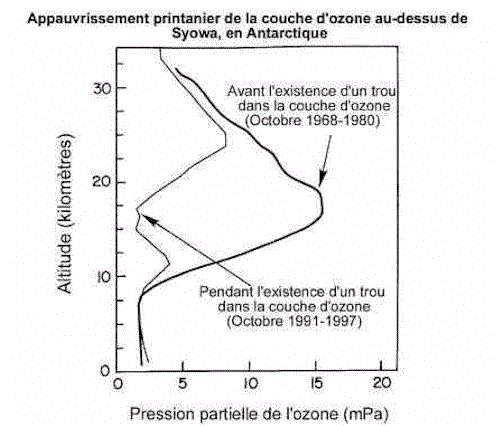
La destruction de l’ozone stratosphérique est un processus complexe, qui fait intervenir de nombreux facteurs. Elle est accélérée par la présence de niveaux significatifs de catalyseurs(7), plus précisément le chlore et le brome, qui sont membres de la famille des halogènes, des éléments extrêmement réactifs. Le chlore et le brome présents dans la stratosphère proviennent de nombreuses sources, tant humaines que naturelles. La principale source des halogènes dans l’atmosphère est constituée de produits de synthèse appelés « halocarbures »(8), qui contribuaient pour 82 p. 100 au chlore pénétrant dans la stratosphère au début des années 1990(9). Les halogènes de source naturelle ont une durée de vie plus courte que les halocarbures. À moins qu’ils ne soient injectés directement dans la stratosphère par une activité volcanique importante, ils sont dissous et lessivés par les précipitations dans les basses régions de l’atmosphère, où interviennent les conditions météorologiques. Les halocarbures ne sont pas solubles dans l’eau; toutes les quantités émises atteignent donc à terme la stratosphère via le mélange atmosphérique, en général sur une période de 5 ans.
Lorsque les halocarbures atteignent la stratosphère, l’exposition au rayonnement ultraviolet de haute énergie et le contact avec d’autres substances chimiques brisent les liaisons entre les atomes, libérant les halogènes qui peuvent se lier chimiquement de nombreuses manières, par exemple en chlorure d’hydrogène ou en nitrate de chlore.
La stratosphère est réputée pour son absence de nuages; pourtant, l’appauvrissement de l’ozone survient surtout dans les nuages stratosphériques polaires (PSC), des nuages nocturnes lumineux composés d’eau en surfusion et d’acides nitrique et sulfurique. Les PSC se forment à de basses températures et constituent des sites actifs(10) dans lesquels une réaction très lente en phase gazeuse peut se faire très rapidement dans un processus hétérogène, c’est-à-dire sur des surfaces solides. Lorsqu’il y a des PSC, le chlore qui est séquestré, par des ions hydrogène(11) ou des oxydes d’azote(12), est libéré sous la forme de chlore gazeux (Cl2), produisant de l’acide nitrique(13). Plusieurs autres réactions hétérogènes se déroulent aussi dans les PSC, et contribuent à l’appauvrissement de l’ozone.
Le chlore moléculaire est dissocié par le rayonnement solaire après la fin de la nuit polaire. Les atomes de chlore réagissent avec l’ozone (O3) pour former du monoxyde de chlore (ClO) et de l’oxygène moléculaire (O2). Le monoxyde de chlore se combine alors avec l’oxygène atomique (O), libéré dans le processus naturel de création de l’ozone, pour donner de l’oxygène moléculaire (O2) et régénérer du chlore atomique (Cl). De façon générale, lorsque les conditions y sont favorables, un seul atome de chlore, agissant comme catalyseur, peut détruire jusqu’à 100 000 molécules d’ozone, sur une centaine d’années.
Ce sont les régions polaires qui connaissent le plus grand nombre de PSC, à cause d’un phénomène connu sous le nom de « vortex polaire ». Cette zone d’air stratosphérique extrêmement froid en rotation autour du pôle se forme pendant la longue nuit polaire. Le vortex empêche l’apport, et le mélange atmosphérique, d’ozone stratosphérique ou de chaleur. La perte d’ozone survient rapidement sur ces plates-formes lorsque le rayonnement solaire revient et photolyse(14) les molécules de chlore. Souvent, les particules des PSC qui contiennent de l’azote grossissent(15) et s’installent à un niveau plus bas (ce processus est appelé dénitrification). Par conséquent, le chlore n’est plus séquestré par les oxydes d’azote, mais la destruction catalytique de l’ozone se poursuit(16).
Le relief de l’Antarctique étant généralement uniforme, le vortex polaire austral est plus intense que celui de l’Arctique. Au-dessus de certaines zones de l’Antarctique, la baisse de l’ozone peut atteindre 70 p. 100 en l’espace de quelques semaines(17).
Les conséquences environnementales de l’appauvrissement de l’ozone sont de deux ordres : le bilan énergétique radiatif de la Terre est altéré, et la quantité de rayonnement ultraviolet nocif qui atteint la surface de la planète augmente.
A. Équilibre du rayonnement thermique
L’ozone joue un rôle dans la régulation du flux de chaleur dans l’atmosphère en absorbant le rayonnement du soleil. La distribution exacte de l’ozone dans la stratosphère influe donc sur la température de l’atmosphère et sur les régimes météorologiques. Même de petits changements de l’apport d’énergie solaire dans l’atmosphère ou de l’échange radiatif d’énergie entre le sol et l’atmosphère peuvent modifier le climat(18). La distribution de la température dans la stratosphère est une fonction directe de celle de l’ozone(19). Cet état de choses a beaucoup d’importance parce que l’appauvrissement de l’ozone est très sensible à la température.
L’énergie émise par le Soleil couvre un large spectre. Une partie est sous la forme d’énergie ultraviolette, qui a une longueur d’onde plus courte que celle de la lumière violette. La partie du spectre ultraviolet composée des longueurs d’onde de 280 à 320 nanomètres (ou 10-9 m), appelée ultraviolet-B (UV-B), est dangereuse en quantités excessives. Les UV-C sont encore plus énergétiques, mais sont presque entièrement filtrés par l’ozone. Un appauvrissement de la couche d’ozone fait monter l’intensité des UV-B au niveau du sol d’environ le double de la baisse en pourcentage, tous autres facteurs exclus. Par exemple, si l’ozone est appauvri de 30 p. 100, la quantité d’UV-B atteignant la surface de la Terre augmente de 60 p. 100(20).
Sous des quantités élevées d’UV-B, les matériaux synthétiques comme les plastiques, et les matériaux naturels comme le bois, changent de couleur et se détériorent plus vite. De nombreuses autres catégories de matériaux pourraient être touchés de même; les recherches à ce sujet se poursuivent.
1. Incidence sur la santé humaine
Le rayonnement ultraviolet peut briser les liaisons chimiques de diverses substances, dont l’ADN, les molécules qui codent l’information génétique. Les effets du rayonnement UV sont complexes et difficiles à interpréter, mais plusieurs conséquences de l’exposition de l’être humain à des niveaux accrus d’UV-B ont été confirmées.
L’exposition excessive au rayonnement UV-B, surtout pendant l’enfance, cause une augmentation des cas de cancer de la peau. Une des raisons en est que les UV-B affectent les réactions immunitaires de la peau, de sorte que l’organisme est moins susceptible de rejeter une tumeur en train de grossir(21). On s’attend à ce qu’une diminution de 10 p. 100 de l’ozone stratosphérique total entraîne chaque année, à l’échelle de la planète, une augmentation de 300 000 du nombre de cancers de la peau avec mélanome bénin et de 4 500 de celui de cancers avec mélanome malin(22). Sans les dispositions du Protocole de Montréal (voir ci-dessous la section « Mesures internationales »), l’appauvrissement de l’ozone aurait fait chaque année 20 millions de cas additionnels de cancer de la peau(23).
Comme le rayonnement ultraviolet affaiblit le système immunitaire, surtout dans les cellules cutanées, les maladies infectieuses dont un stade implique la peau vont probablement augmenter. De plus, l’efficacité des vaccins contre les maladies infectieuses peut se trouver réduite(24).
Une exposition répétée à des niveaux excessifs de rayonnement UV peut aussi sensibiliser les yeux à développer des cataractes, principale cause de cécité dans le monde. On estime que 20 p. 100 des cataractes sont dues à une exposition aux UV(25). Parmi les autres effets confirmés figurent la myopie liée à l’âge et la déformation de la capsule du cristallin.
Afin de réduire les risques pour la santé, les gens peuvent prendre un certain nombre de mesures, comme d’appliquer des écrans solaires avec un facteur de protection d’au moins 15, de porter des chapeaux et des vêtements protecteurs, de rester le plus possible à l’ombre, et de porter des lunettes de soleil de bonne qualité traitées pour absorber le rayonnement UV-B. En prenant les bonnes précautions, on peut réduire à un minimum les effets négatifs de l’appauvrissement de la couche d’ozone sur la santé.
2. Incidence sur la flore terrestre
L’exposition accrue au rayonnement ultraviolet peut avoir des effets très marqués sur les végétaux, dont elle affecte les hormones et la croissance. Parmi les effets particuliers observés figurent :
une réduction du poids sec total, de la teneur en éléments nutritifs et de la surface foliaire disponible pour la photosynthèse;
une détérioration de la qualité de certains types de tomates, de légumineuses, de choux, de pommes de terre et de betteraves à sucre;
une baisse des taux de floraison ou de germination;
une modification de la distribution des éléments nutritifs dans la plante.
Alors que, pour certaines cultures, comme le soja, une augmentation de l’exposition aux UV-B entraîne une baisse de la production, nombre d’autres ne sont pas affectées, ou montrent une tolérance élevée. Les recherches indiquent que, chez certaines plantes (p. ex. le semis de seigle, de maïs et de tournesol), la croissance et la photosynthèse peuvent être inhibées même sous les niveaux ambiants d’UV-B(26).
Les mécanismes de protection naturels de nombreux organismes pourraient ne pas être suffisants contre des niveaux plus élevés de rayonnement UV. (On a des indications que certaines mauvaises herbes résistent mieux aux UV que les cultures.) Les tests d’exposition ont montré que plus de 100 espèces de plantes terrestres pourraient être sensibles aux augmentations du rayonnement UV dues à l’appauvrissement de l’ozone stratosphérique. Des recherches internationales ont révélé que certaines espèces de riz sont affectées par des accroissements même mineurs des UV-B. Des recherches menées en vue de sélectionner et de cultiver efficacement des espèces fortes pourraient aider à compenser certains des effets dommageables.
Étant que chaque essence d’arbre ou autre espèce végétale a sa sensibilité propre aux UV, la diversité et la répartition de ces espèces pourraient changer; il est même possible que certaines disparaissent(27). Des études montrent en effet que de nombreuses espèces de conifères souffrent d’une augmentation du rayonnement UV-B.
On sait par ailleurs qu’une augmentation des niveaux naturels d’UV-B induit des mutations dans les micro-organismes. Cependant, avec la possibilité de mutations plus rapides, on pourrait constater une adaptation rapide au stress causé par les UV-B. Bien que certaines recherches indiquent qu’une adaptation limitée est possible, la majorité des effets demeurent très négatifs. À l’échelle planétaire, une baisse du taux de fixation de l’azote atmosphérique par les champignons exigerait, en compensation, un recours accru aux engrais de synthèse(28). Les composés azotés, produits en grandes quantités par les micro-organismes du sol, semblent jouer un rôle important dans les fluctuations naturelles des niveaux d’ozone(29).
3. Incidence sur la vie aquatique
Tous les éléments de la biosphère semblent affectés à un degré quelconque par l’augmentation des UV-B. Le phytoplancton (phyto = plante) est très sensible au rayonnement ultraviolet; il ne dispose en effet pas des couches protectrices des organismes supérieurs et dérive à la surface des eaux, où il peut être exposé aux UV-B. En plus d’être la base du réseau trophique aquatique, le phytoplancton est un important producteur d’oxygène et un puits du carbone, dont on sait qu’il absorbe de grandes quantités de dioxyde de carbone atmosphérique. Le phytoplancton marin produit au moins autant de biomasse que tous les écosystèmes terrestres réunis. Des changements dans la production de phytoplancton pourraient donc exacerber l’effet de serre.
Des scientifiques de l’université de Plymouth ont constaté que les cellules reproductrices des algues sont plusieurs fois plus sensibles au rayonnement ultraviolet que les cellules à maturité. Des recherches en laboratoire ont montré que les spores asexuées des espèces étudiées étaient 6 fois plus sensibles aux UV-B que le plancton à maturité. Les gamètes flottants, mode sexué de reproduction, étaient encore plus susceptibles. L’impact écologique pourrait être maximal à certaines périodes du printemps, pendant les épisodes de « fleurs d’eau », lorsque la reproduction du plancton est la plus intense(30). Il est difficile d’évaluer ces effets sur le phytoplancton, parce qu’on manque de données décrivant les niveaux d’UV-B et d’activité biologique pour la période antérieure à l’appauvrissement de la couche d’ozone.
Le zooplancton (zoo = animal) – composé de petits organismes, comme des larves de poissons et de crustacés – est en péril, de même que les anchois, parce qu’ils passent des périodes critiques de leur cycle biologique près de la surface de l’eau, à une profondeur où les UV-B peuvent les atteindre. Une réduction de l’abondance de ces organismes, situés près de la base du réseau trophique, pourrait entraîner une réduction des populations de poissons. Et cette situation pourrait avoir des répercussions désastreuses sur la disponibilité de la nourriture à l’échelle de la planète. Le poisson contribue pour 18 p. 100 aux protéines animales de la planète, et pour 40 p. 100 aux protéines consommées en Asie(31). Les écosystèmes dulcicoles sont eux aussi menacés par une intensification de l’exposition aux UV-B(32).
L’on s’entend assez bien sur le fait que les augmentations des UV-B liées à l’appauvrissement de l’ozone peuvent avoir une large gamme d’effets, directs comme indirects, sur les écosystèmes aquatiques, surtout dans les régions polaires, où les formes de vie sont moins adaptées à une lumière solaire intense. Les études montrent généralement que l’augmentation du rayonnement UV sous le trou d’ozone de l’Antarctique fait baisser de 6 à 12 p. 100 la production de plancton pendant la période d’exposition. On a fait la preuve de dommages aux niveaux des molécules, des cellules, des populations et des communautés.
4. Incidence sur la pollution atmosphérique
Les changements atmosphériques découlant de l’augmentation du rayonnement UV-B sont particulièrement préoccupants. On a constaté une baisse de la qualité de l’air dans la troposphère, le niveau inférieur de l’atmosphère. La réactivité chimique dans la troposphère augmente en réponse à l’accroissement des UV-B, ce qui fait monter les niveaux de pollution atmosphérique. Les UV-B stimulent la formation de molécules qui réagissent rapidement avec d’autres substances pour en créer de nouvelles. Par exemple, il se forme des radicaux hydroxyle, qui contribuent à la production d’ozone troposphérique, d’aérosols et d’autres polluants dangereux. Dans les régions urbaines, une réduction de 10 p. 100 de la couche d’ozone induira probablement une augmentation de 10 à 25 p. 100 de l’ozone troposphérique. Le smog exposé au rayonnement contribue à l’apparition de substances organiques(33) oxydées, comme les formaldéhydes. Ces molécules ont tendance à produire des radicaux hydrogène réactifs, qui contribuent à la formation de peroxyde d’hydrogène. Le peroxyde d’hydrogène est la principale substance qui oxyde le dioxyde de soufre en acide sulfurique dans l’eau des nuages, ce qui lui confère un rôle important dans la formation des pluies acides(34).
Chaque année, l’appauvrissement printanier de l’ozone sur l’Antarctique est plus marqué (figure 3), et les moyennes annuelles plus basses que la normale. Le trou d’ozone de 2000 a été le plus vaste jamais constaté en Antarctique, s’est formé deux semaines plus tôt qu’à l’habitude et s’est étendu au-delà du vortex polaire(35).
Figure 3(36)
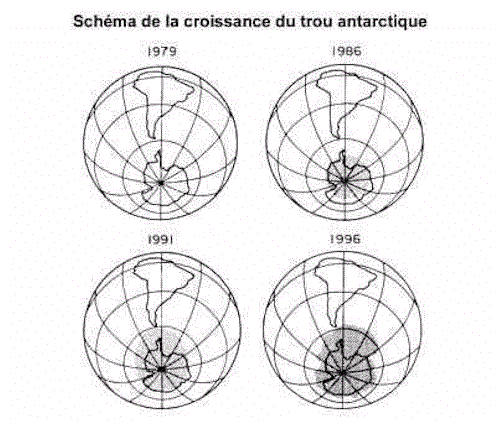
Dans l’Arctique, l’appauvrissement de l’ozone est survenu de façon moins brutale que dans l’Antarctique. Le vortex polaire arctique se dissipe habituellement à la fin de l’hiver, avant le retour de la lumière solaire. Les épisodes d’appauvrissement significatif de l’ozone y deviennent cependant plus fréquents. De nombreux projets internationaux, faisant intervenir des satellites, des aéronefs volant à haute altitude, des ballons et des stations au sol, aident à améliorer la compréhension des processus qui régissent la production, l’appauvrissement et la distribution de l’ozone. On a recours à diverses techniques pour détecter et mesurer les facteurs en jeu. Le satellite de recherche sur la haute atmosphère (Upper Atmosphere Research Satellite, ou UARS) de la NASA a été lancé en septembre 1991. Il a été configuré pour mesurer les concentrations de substances destructrices de l’ozone, ainsi que les taux d’ozone, à diverses altitudes. L’instrument américain TOMS (pour Total Ozone Mapping Spectrometer, ou spectromètre imageur de l’ozone total), embarqué sur satellite, est utilisé pour déduire les niveaux de l’ozone du rayonnement solaire rétrodiffusé dans le spectre UV.
L’Expérience de surveillance de l’ozone (Global Ozone Monitoring Experiment, ou GOME), dont l’équipement a été lancé en avril 1995 sur la plate-forme européenne ERS-2, a marqué le début d’un programme de surveillance à long terme de l’ozone. Les scientifiques reçoivent ainsi des données de grande qualité sur la distribution planétaire de l’ozone et de plusieurs gaz traces influant sur le climat et présents dans l’atmosphère de la Terre. GODIVA (Global Ozone Data Interpretation, Validation and Application, ou Interprétation, validation et application des données mondiales sur l’ozone) est un volet de GOME, et contribue aussi à d’autres expériences comme la campagne THESEO 2000 (pour Third European Stratospheric Experiment on Ozone 2000, ou troisième expérience stratosphérique européenne sur l’ozone) et le volet Expérience sur la perte d’ozone et la validation (Ozone Loss and Validation Experiment) de SAGE III (SOLVE), qui ont été menés conjointement. À ces expériences ont participé plus de 350 chercheurs venus des États-Unis, d’Europe, de Russie, du Japon et du Canada. Les résultats de ces projets confortent la théorie que le rétablissement de la couche d’ozone pourrait être retardé, en raison d’un renforcement du vortex polaire et d’un refroidissement de la stratosphère.
Environnement Canada participe à diverses expériences liées à la chimie de l’ozone, comme l’Initiative pour l’atmosphère moyenne, dans un but de modélisation, d’assimilation des données et de surveillance de cette région de l’atmosphère(37). Un satellite canadien (SCISAT-1) de l’Expérience sur la chimie de l’atmosphère devrait être lancé en 2002 pour étudier l’appauvrissement de l’ozone à l’échelle planétaire(38).
L’analyse des données satellitaires révèle que la perte d’ozone dans l’hémisphère Nord se produit maintenant plus rapidement qu’on ne l’avait prévu. Bien que les pertes d’ozone dans l’Arctique n’aient encore jamais été comparables à celles de l’Antarctique, elles y ont considérablement augmenté au cours des années 1990. Des pertes isolées proches de 45 p. 100 portent à s’inquiéter, la population humaine étant plus nombreuse dans cette région qu’au pôle Sud(39).
On s’attend à ce que, aux deux pôles, la perte d’ozone continue d’augmenter au cours des prochaines décennies avant que la couche d’ozone se rétablisse. Il a été récemment découvert que les gaz à effet de serre entraînent un refroidissement plus prononcé de la haute atmosphère(40). Les modèles informatiques prédisent que, du fait des changements des températures et des vents induits par les émissions de gaz à effet de serre, il se formerait au-dessus de l’Arctique un vortex plus intense et de plus longue durée.
SUBSTANCES DESTRUCTRICES DE L’OZONE
Lorsqu’on a commencé à se préoccuper de la couche d’ozone, dans les années 1970, l’attention s’est d’abord portée sur des aéronefs avancés, que l’on soupçonnait d’être à l’origine du problème, puis est passée aux plus prosaïques contenants aérosols. Les substances chimiques industrielles connues sous le nom du groupe des CFC (chlorofluorocarbures) étaient alors utilisées comme agent propulseur. Des milliers de tonnes de CFC étaient libérées directement dans la basse atmosphère, d’où ils commençaient à s’élever graduellement pour aller détruire l’ozone stratosphérique. Depuis lors, la liste des substances dont on sait qu’elles attaquent l’ozone stratosphérique s’est considérablement allongée.
On mène encore des recherches sur l’incidence des aéronefs pour ce qui est de l’appauvrissement de la couche d’ozone(41). Des études ont montré qu’il faudrait améliorer l’efficacité et les stratégies de gestion pour réduire l’impact de l’aviation sur la couche d’ozone(42). Des mesures en vol des émissions des avions supersoniques ont grandement contribué à améliorer la fiabilité des études sur les effets de cette forme de transport sur l’ozone stratosphérique(43). Il convient de s’inquiéter des émissions de composés azotés (NO et NO2) par les avions supersoniques, étant donné la haute altitude des vols et l’accroissement inéluctable de la flotte aérienne.
Les CFC, et les autres agents destructeurs de l’ozone, sont omniprésents dans presque toutes les sociétés. Ils sont utilisés dans une large gamme de produits que l’on n’associe généralement pas à des substances appauvrissant la couche d’ozone. Étant donné la multitude de matières en jeu, on a adopté la notion de « potentiel de destruction de l’ozone » (PDO) pour déterminer le potentiel qu’a une substance de détruire l’ozone, sur une base de masse par kilogramme, le PDO de référence de 1 étant attribué au trichlorofluorométhane, appelé CFC-11 dans le système de classification conventionnel. Le PDO est fonction de divers facteurs, comme la durée de vie atmosphérique de la substance, son poids moléculaire, sa capacité de dissociation photolytique, et d’autres dont on sait qu’ils donnent une estimation précise du potentiel relatif de destruction de l’ozone.
Le tableau en annexe donne la liste de nombreux agents d’appauvrissement de l’ozone, avec leurs PDO, ainsi que de certains produits de remplacement des CFC. Les hydrochlorofluorocarbures (HCFC), qui remplacent actuellement les CFC, ont un bas PDO; les hydrofluorocarbures (HFC) ont un PDO de zéro et ne sont donc pas énumérés. Les recherches se poursuivant, des PDO sont mis à jour à l’occasion. Certaines durées de vie sont encore en train d’être mesurées. Le PNUE évalue les progrès réalisés par un pays pour atteindre les objectifs en mesurant la production de groupes de substances appauvrissant la couche d’ozone en tonnes de PDO (tonnes métriques multipliées par le PDO).
Quantitativement, ce sont les CFC qui ont été les principaux agents destructeurs de l’ozone. Étant donné qu’ils sont stables, non toxiques, ininflammables et à l’épreuve de la corrosion, on les a utilisés comme réfrigérants, propulseurs d’aérosols, solvants et agents de gonflement des mousses. Des technologies de remplacement ont été développées pour nombre de ces applications, et le défi est maintenant de faire en sorte que les grandes quantités de CFC qui ont été utilisées en réfrigération et en climatisation soient régénérées, au lieu de les laisser s’échapper dans l’atmosphère.
L’autre grand groupe de destructeurs de l’ozone est celui des halons, qui sont de composition similaire à celle des CFC, mais contiennent du brome. On utilise encore des halons dans la lutte contre les incendies pour de nombreuses raisons : ils sont peu toxiques, ne nuisent pas à la visibilité pendant l’utilisation, laissent peu de résidus corrosifs ou abrasifs, et ont une excellente efficacité (mesurée selon le poids utilisé). Bien que la production de halons dans les pays industrialisés ait largement diminué depuis 1994, les concentrations stratosphériques de ces puissants destructeurs d’ozone continuent d’augmenter, du fait de leurs longues durées de vie atmosphériques et du temps requis pour le mélange atmosphérique. Dans les pays en développement, aucune restriction ne s’applique aux halons jusqu’à janvier 2002. Les halons ont un potentiel de destruction de l’ozone extrêmement élevé (trois à dix fois plus grand que celui des CFC), et l’usage auquel on les destine entraîne leur rejet direct dans l’atmosphère. Les autres agents – comme le tétrachlorure de carbone, le méthyle chloroforme et le bromure de méthyle – ont été utilisés à diverses fins, par exemple comme matière de base pour la production de CFC, dans des pesticides et dans des solvants de nettoyage à sec.
En 1997, la charge globale d’halocarbures dans la stratosphère – ou équivalent chlore effectif (EClE) – a commencé à baisser, surtout en raison de l’élimination graduelle du trichloroéthane, un solvant de nettoyage. Comme il a une durée de vie relativement courte (4,8 ans), il est maintenant très peu présent dans la stratosphère. Sans ce facteur, l’EClC continuerait de monter; il pourrait cependant ne pas baisser beaucoup plus, à moins que les émissions de substances appauvrissant la couche d’ozone (SACO) puissantes et de longue durée de vie ne baissent davantage d’ici 2010. La substance chimique qui contribue actuellement le plus à l’EClE dans l’atmosphère est le halon-1211. Son abondance dans la stratosphère est restée relativement constante, malgré les limites imposées à sa production dans les pays développés(44).
La nécessité de réduire l’utilisation de substances appauvrissant la couche d’ozone s’est traduite par de nombreuses innovations technologiques et par l’utilisation de substances de remplacement pour chaque application. Parmi les innovations dignes de mention figurent de nouveaux propulseurs, solvants, agents moussants, agents extincteurs et techniques de lutte antiparasitaire(45). Cet urgent besoin de changement a également imposé de faire progresser les technologies de récupération et de recyclage. Les changements les plus importants et les plus difficiles sont survenus dans le domaine de la réfrigération et de la climatisation. La plupart des recherches ont donc visé à trouver des substituts pour les CFC en tant que réfrigérants.
L’utilisation des CFC a été grandement réduite dans les pays industrialisés. De nombreux substituts faisaient appel à des HCFC et, jusqu’à un certain point, à des HFC. C’est en 1991 qu’on a pour la première fois utilisé le HFC-134 dans les climatiseurs d’automobiles, et cet usage s’est rapidement répandu. L’un des problèmes des HCFC et des HFC est qu’ils ont une efficacité énergétique inférieure à celle des CFC. DuPont, plus important producteur de CFC du monde, a cessé d’en fabriquer en 1993, cinq ans plus tôt que prévu au départ, et fabrique maintenant des HCFC et des HFC. Les HCFC sont de très puissants gaz à effet de serre et, aux termes d’amendements au Protocole de Montréal, ils doivent être éliminés graduellement d’ici 2030 dans les pays développés. Certains HFC ont aussi un fort potentiel de réchauffement du globe et de longues durées de vie atmosphérique.
Un progrès intéressant dans la solution du problème des réfrigérants est la mise au point du réfrigérateur thermo-acoustique, qui n’a pas de pièces mobiles et utilise des gaz sans danger pour l’environnement. Bien qu’il soit basé sur un principe simple, sa conception est en fait complexe. Un haut-parleur à l’extrémité d’un tube rempli de gaz produit un son qui y résonne, générant une onde stationnaire(46), qui transmet la chaleur vers le ventre de l’onde(47)(48). Comme cette vibration est contrôlée avec précision, les réfrigérateurs thermo-acoustiques seront moins bruyants que les modèles classiques. Une récente démonstration au Los Alamos National Laboratory a montré que l’on pouvait simplifier les choses en éliminant l’échangeur thermique froid et en refroidissant à la place le gaz à action thermo-acoustique(49).
Autre invention intéressante : le réfrigérateur magnétique, mis au point par l’Astronautics Corporation of America dans le cadre d’un contrat avec le département de l’Énergie des États-Unis. Il a une efficacité énergétique comparable à celle des appareils classiques. Bien que le coût de l’aimant au gadolinium soit un obstacle important à son utilisation généralisée, il sera probablement mis en marché dans un avenir proche pour les grandes entreprises commerciales(50).
Parmi les autres solutions figurent des appareils avec une plus petite quantité mais une plus grande superficie de couverture du refroidissant. Une technique peu coûteuse mais fort utile pour les applications dans le désert a récemment valu à Mohammed Bah Abba, du Nigéria, le prix Rolex à l’esprit d’entreprise. Le système, basé sur les propriétés refroidissantes de l’évaporation, utilise du sable humide entre deux pots d’argile(51). Le rayonnement ionisant est aussi une technique de remplacement pour la conservation des denrées alimentaires(52).
L’ammoniac est couramment utilisé comme réfrigérant dans l’industrie, pour les installations d’entreposage au froid et dans le secteur pétrochimique, entre autres. Les inconvénients de ce réfrigérant sont sa corrosivité et son inflammabilité à certaines concentrations dans l’air. Des rejets accidentels, exacerbés par la pressurisation de ce système de réfrigération, ont entraîné des blessures et des décès consécutifs à l’inhalation des vapeurs, ainsi que des cas de contamination de l’eau(53). Pour ce qui est de la couche d’ozone, l’ammoniac entrerait dans des composés stables avant d’atteindre la stratosphère.
Pour remplacer les CFC dans la production de mousses, dont les utilisations vont de l’isolation à la confection de tasses, on a par exemple réduit la quantité de propulseur requis et remplacé les CFC par des HCFC, moins dommageables. Après de nombreuses années de recherches, l’entreprise The Lily Cup Inc., de Toronto, a mis au point une technique novatrice qui utilise comme agent moussant de l’oxygène et du dioxyde de carbone recyclé(54).
Des changements ont été apportés même dans le secteur des soins de santé. Par exemple, les hôpitaux ont réduit leur consommation de CFC comme agents stérilisants. Le Canada est en train d’éliminer graduellement, d’ici 2005, les CFC utilisés comme propulseurs dans les inhalateurs-doseurs. L’utilisation du premier inhalateur-doseur sans CFC a été approuvée en août 1997. Dans ce produit, le CFC propulseur a été remplacé par un hydrofluoroalcane (HFA), qui ne cause pas d’appauvrissement de l’ozone. La sécurité des HFA dans les utilisations médicales a été démontrée par des tests très poussés. L’utilisation de l’inhalateur-doseur sans CFC a maintenant été approuvée dans plus de 35 pays(55).
L’industrie de l’électronique était un des principaux utilisateurs de solvants à base de CFC. Pour la plupart des applications, on a mis au point de nouveaux solvants sans CFC. En 1991, Northern Telecom a élaboré et mis en œuvre une technologie de remplacement pour souder les cartes de circuits électroniques sans devoir au préalable utiliser de solvants(56). L’entreprise a co-fondé la Coopérative industrielle pour la protection de la couche d’ozone (maintenant devenue l’International Co-operative for Environmental Leadership), qui met en commun les nouvelles technologies. Cette découverte a valu à Northern Telecom l’Appropriate Technology Award du Financial Post en 1993(57). De nombreux fabricants de matériel électronique ont maintenant cessé d’utiliser des CFC.
Le traitement thermique, l’utilisation de la terre de diatomées ou l’utilisation d’organismes vivants dans la lutte antiparasitaire permettent de remplacer le bromure de méthyle pour la fumigation des fruits et légumes et des cultures. La compagnie canadienne Knowzone Solutions Inc. a récemment acquis les droits de la technologie Bromosorb® pour le piégeage du bromure de méthyle après la fumigation.
La société Sécuriplex, du Canada, a mis au point plusieurs substituts des halons dans la lutte contre l’incendie, produits qui éteignent rapidement les feux sans endommager les équipements.
MESURES VISANT LA RÉDUCTION DES AGENTS DESTRUCTEURS
La communauté internationale a relevé le défi de mettre fin à la destruction de la couche d’ozone stratosphérique. C’est là l’une des principales raisons de la rapidité du développement technologique de substituts des CFC. Le Canada, qui participe très activement aux discussions internationales, a été parmi les premiers à agir. En mars 1980, il a interdit l’utilisation des CFC dans la plupart des aérosols courants, comme les laques à cheveux, les désodorisants et les antisudorifiques.
En 1985, la Convention de Vienne pour la protection de la couche d’ozone demandait des mesures volontaires pour réduire les émissions de substances destructrices de l’ozone(58). Le Canada a été le premier État à ratifier la Convention de Vienne, en juin 1986. Des mesures plus globales ont été acceptées depuis cette première importante entente internationale.
Donnant une démonstration sans précédent de coopération mondiale, des États du monde entier se sont engagés à prendre des mesures strictes pour protéger la couche d’ozone. En septembre 1987, ils ont adopté le Protocole de Montréal, qui comportait un calendrier de réduction et, à terme, d’élimination de la production de CFC et de halons. Le Protocole de Montréal, qui est entré en vigueur le 1er janvier 1989, fonctionne avec un système de barrières commerciales régissant l’approvisionnement en SACO, tout en permettant le transfert entre les Parties d’exemptions pour utilisations essentielles. L’application des clauses du Protocole de Montréal a permis de faire plafonner l’abondance des substances chlorées dans la stratosphère.
Des amendements au Protocole ont :
accéléré le calendrier de l’élimination progressive des composés chimiques détruisant l’ozone dans la stratosphère;
ajouté de nouvelles SACO à la liste;
modifié les exigences concernant les exemptions pour utilisations essentielles.
Dès même la signature du Protocole de Montréal, on était conscient qu’il devrait être assorti de contrôles plus stricts, qui ont été adoptés à la conférence de Londres, en 1990. La liste des substances régies par le Protocole s’est allongée de dix, dont le méthyle chloroforme et le tétrachlorure de carbone. Les dates d’élimination ont été fixées à 2000 et 2010 respectivement pour les pays industrialisés et les pays en développement. De nombreuses Parties à cette conférence se sont engagées à éliminer les CFC au plus tard en 1997, soit trois ans avant l’échéance internationale. L’amendement incluait la création d’un fonds destiné à aider les pays en développement visés par l’article 5 du Protocole. Le Fonds multilatéral a ainsi pu aider les pays en développement à passer à des substances et technologies moins nocives pour l’ozone, en leur fournissant une assistance financière, de la formation et des informations technologiques. Les organismes internationaux responsables de la mise en œuvre du Fonds multilatéral sont :
le Programme des Nations Unies pour l’environnement (PNUE);
le Programme des Nations Unies pour le développement (PNUD);
l’Organisation des Nations Unies pour le développement industriel (ONUDI);
la Banque mondiale.
L’amendement de Copenhague de 1992 a resserré le calendrier, de sorte que les pays industrialisés devaient avoir éliminé les CFC, le tétrachlorure de carbone et le méthyle chloroforme en 1996, et les halons en 1994. Le bromure de méthyle et les hydrobromofluorocarbures (HBFC), ainsi que les hydrochlorofluorocarbures (HCFC), ont également été ajoutés à la liste des substances qui devaient être éliminées, respectivement, en 1996 et 2030. Cet amendement renforçait aussi les contrôles commerciaux et les procédures applicables en cas de non-conformité.
Les ajustements de Vienne de 1995 ont gelé la production et la consommation de bromure de méthyle aux niveaux de 1995-1998 et prévoyaient de geler les niveaux de consommation des HCFC en 2016.
L’amendement de Montréal, élaboré en 1997, a fait passer les échéances d’élimination du bromure de méthyle à 2005 et 2015, respectivement, pour les pays industrialisés et les pays en développement. Un nouveau système de permis faisant intervenir l’échange régulier d’information entre les Parties a été mis au point pour faire cesser le commerce illégal des SACO.
Les initiatives de l’amendement de Beijing de décembre 1999, que le Canada a été l’un des premiers pays à accepter, doivent encore être ratifiées par les 20 pays requis pour qu’il puisse entrer en vigueur. L’amendement inclut de nouvelles limites à la production de HCFC, gelant la production aux niveaux de 1989 en 2004 en vue d’une élimination en 2030 pour les pays industrialisés, et d’un gel aux niveaux de 2015 en 2016 pour les pays en développement(59). Le nouvel amendement interdit aussi à partir de 2004 le commerce des HCFC avec les pays qui n’ont pas encore ratifié l’amendement de Copenhague de 1992. L’élimination d’une SACO récemment mise au point, le bromochlorométhane, doit être réalisée par tous les pays en 2002. En même temps, le comité exécutif du Fonds multilatéral a décidé d’augmenter l’aide accordée à l’Inde et à la Chine pour réduire leur production au cours des 10 prochaines années. Ces pays ont en effet de la difficulté à atteindre leurs objectifs de réduction(60).
Les importations de CFC et halons nouvellement produits par les pays industrialisés ont en grande partie été interdites, de même que les importations et exportations d’autres SACO puissantes. Les substances destructrices de l’ozone existantes sont réutilisées et recyclées chaque fois que c’est possible. L’article 5 du Protocole accorde un délai de grâce aux pays en développement dans la mesure où leurs utilisations de SACO n’augmentent pas de façon significative. Ces Parties ont maintenu leur production de CFC aux niveaux de référence de 1995-1997, et entreprennent de réduire l’utilisation de ces substances de 50 p. 100 d’ici 2005.
Des pays d’Europe de l’Est et de grands pays d’Asie – comme la Russie, la Chine et l’Inde – ont de la difficulté à passer aux technologies de réfrigération avancées. Grâce à la collaboration, les changements essentiels sont en train de se faire juste au moment où ces importantes populations commencent à profiter pleinement de ces technologies utiles. À l’heure actuelle, la Chine est le plus gros producteur de CFC et de halons de la planète. Le Fonds pour l’environnement mondial, par l’entremise du PNUD, a aidé à éliminer graduellement les installations de production de CFC de la Russie et à moderniser la fabrication des appareils en Chine(61) et en Inde; ces deux pays commencent à produire des réfrigérateurs qui utilisent des hydrofluorocarbures et de l’isobutane(62).
En 1997, on estimait à 235 milliards de dollars US les coûts totaux des mesures prises pour protéger la couche d’ozone. Cependant, les effets nocifs sur les pêches, l’agriculture et les matériaux que l’on a ainsi évités sont à eux seuls estimés au double de ce montant(63).
B. Initiatives du gouvernement fédéral
Le Canada a modifié le Règlement sur les substances appauvrissant la couche d’ozone (SACO), 1998, pris en application de la Loi canadienne sur la protection de l’environnement, à compter de janvier 2001, pour tenir compte des amendements au Protocole de Montréal, améliorer la réglementation des SACO et régler des problèmes administratifs.
Le règlement fédéral interdit la production et l’importation de CFC et de halons dans la plupart des cas, et fixe des balises strictes aux exportations. L’actuel règlement fédéral interdit l’importation et l’exportation de halons récupérés, sauf aux termes d’un permis.
Les restrictions visant le remplissage de l’équipement encouragent la conversion à des solutions de remplacement. La transition est facilitée par l’imposition d’une baisse de l’approvisionnement, qui fait que le coût des CFC augmente régulièrement alors que celui de ses substituts baisse. La figure ci-dessous présente les réductions de la consommation de SACO au Canada.
Figure 4(64)
CONSOMMATION CANADIENNE DE SACO (en kilotonnes)
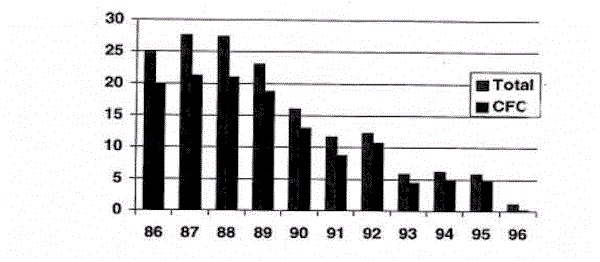
* toutes les quantités sont pondérées en fonction du PDO
En 1996, les fabricants ont commencé à utiliser des réfrigérants de remplacement pour le nouvel équipement. Cependant, un grand nombre d’appareils contenant des CFC sont restés sur le marché jusqu’à récemment. Ces appareils ont une longue durée de vie utile (environ 13 à 15 ans). Le stock de CFC devrait être disponible pour l’entretien des appareils ménagers jusqu’en 2020.
La production de tétrachlorure de carbone, de méthyle chloroforme et de bromure de méthyle a été arrêtée graduellement dans les pays industrialisés et, au Canada, il ne reste pas de surplus important à gérer.
À l’heure actuelle, le Canada a une seule installation d’incinération permanente approuvée pour l’élimination des SACO, située à Swan Hills, en Alberta. Comme elle a une capacité limitée, le Canada peut permettre que des SACO soient exportées à l’étranger pour y être détruites dans une installation appropriée. Des installations capables de détruire les SACO sont présentement en service en Australie, en Suède, en Allemagne, au Japon, au Royaume-Uni, en Russie et aux États-Unis.
Pour que les Canadiens puissent prendre les précautions voulues contre des niveaux accrus d’UV-B, Environnement Canada a annoncé un service d’avis peu après que la NASA a confirmé qu’il y avait une forte possibilité que la couche d’ozone soit substantiellement appauvrie au-dessus d’une grande partie du Canada. Ce service a débuté le 13 mars 1992, beaucoup plus tôt que prévu au départ, et fournit des informations quotidiennes sur les manières d’éviter l’exposition au soleil dans un contexte de hausse des niveaux d’UV-B; le Canada est ainsi le premier pays à émettre pour l’ensemble de son territoire des prévisions quotidiennes du rayonnement UV solaire. L’Indice UV a été imité dans le monde entier, ce qui permet aux populations de limiter leur exposition lorsque le rayonnement nocif est le plus intense(65).
Un réseau national de stations de surveillance assure une veille continue de la couche d’ozone au-dessus du Canada depuis plus de 30 ans. L’existence de ces premiers enregistrements, avant qu’il y ait eu une quelconque influence majeure de l’homme sur la haute atmosphère, est essentielle pour comprendre les changements survenus. Le Centre mondial des données sur l’ozone et les UV (WOUDC) est un des six centres mondiaux de données reconnus qui font partie du programme Veille de l’atmosphère du globe (VAG), qui relève lui-même de l’Organisation météorologique mondiale (OMM). Le WOUDC, exploité par la Division des études expérimentales du Service météorologique du Canada(66), est situé à Toronto.
C. Mesures fédérales-provinciales
Les ententes internationales se sont traduites en objectifs nationaux. Au Canada, le gouvernement fédéral a travaillé en étroite coopération avec les provinces pour mettre en œuvre les changements nécessaires. L’industrie aussi s’y est impliquée de plus en plus. En avril 1989, le Conseil canadien des ministres de l’environnement (CCME) a chargé le Comité consultatif fédéral-provincial (CCFP) de la Loi canadienne sur la protection de l’environnement de coordonner le développement de mesures de limitation pour tous les territoires de compétence. Le CCME a montré le chemin, en organisant la participation des divers ordres de gouvernement à la réduction, à la récupération et au recyclage des CFC. Le 21 août 1990, le CCME a créé un groupe de travail chargé d’élaborer un Plan d’action national pour la récupération, le recyclage et la régénération des chlorofluorocarbures.
En 1992, le CCME acceptait et publiait le Plan d’action national. La rapidité avec laquelle un plan si vaste a été élaboré témoigne du degré de coopération entre les divers gouvernements devant cet important problème environnemental. Le plan définissait six tâches principales, qui ont été exécutées ou sont encore en cours :
imposer – au moyen de règlements provinciaux – la récupération, le recyclage et la régénération des CFC et des HCFC de toutes les utilisations de réfrigération et de climatisation, y compris une interdiction de rejeter délibérément des CFC et des HCFC dans l’atmosphère;
élaborer, en collaboration avec les associations industrielles, des programmes de formation en récupération et en recyclage pour le secteur de l’entretien; la formation devait inclure le code de pratiques fédéral pour la réduction des émissions de CFC, ainsi qu’une formation pratique liée à l’équipement;
caractériser le stock actuel de CFC au Canada, car cette connaissance est nécessaire pour mesurer l’efficacité des activités de récupération/recyclage et planifier des scénarios de destruction finale;
élaborer, avec la participation des associations industrielles et de normalisation, des normes appropriées de qualité des réfrigérants recyclés et de performance de l’équipement de récupération;
faire en sorte que le grand public soit informé du problème et de ses solutions, puisque sa réaction et sa participation sont partie intégrante de la solution;
réviser les normes d’achat/acquisition du gouvernement, y compris les contrats de service, pour assurer la récupération et le recyclage des CFC, des HCFC et des halons.
Le plus récentPlan d’action national pour le contrôle environnemental des substances appauvrissant la couche d’ozone et leurs halocarbures de remplacement (PAN), publié en 1998 par le Conseil canadien des ministres de l’environnement, vise à continuer de réduire les émissions de substances destructrices de l’ozone.
En 1998, le PAN formulait les objectifs suivants :
améliorer la gestion environnementale de toutes les SACO et des halocarbures de remplacement et réduire leurs émissions au cours de l’installation, du fonctionnement, de l’entretien, de la mise au rebut et du déclassement des systèmes et des appareils;
offrir de la cohérence à l’industrie et réduire au minimum les répercussions sur d’autres questions environnementales;
satisfaire à ces besoins nouveaux en révisant les tâches originales, notamment en recourant aux mesures suivantes :
le maintien des tâches originales selon les besoins;
l’élargissement de certaines tâches originales afin d’y inclure les halocarbures de remplacement;
des nouvelles tâches qui tiennent compte du « Code de pratiques environnementales visant l’élimination des émissions de chlorofluorocarbures des systèmes de réfrigération et de conditionnement d’air » révisé et favorisent la récupération des frigorigènes;
des nouvelles tâches qui tiennent compte du « Code de pratiques sur les halons »;
des nouvelles tâches visant d’autres secteurs industriels afin de réduire les émissions de chlorofluorocarbures;
des nouvelles tâches afin de fournir la documentation de base nécessaire à l’évaluation de mesures à venir.
Les gouvernements de toutes les provinces et celui d’un territoire ont mis en place des règlements visant le rejet de SACO, et en imposant la récupération et le recyclage(67).
D. Mesures qui restent à prendre
Lors de la plus récente réunion des Parties, à Beijing, le Secrétaire exécutif du Secrétariat de l’ozone, K. Madhava Sarma, a fait remarquer que la consommation et la production de SACO avaient baissé de près de 90 p. 100, mais qu’il reste des obstacles à surmonter. Il s’agissait d’une croissance des émissions due :
aux exemptions;
à l’accroissement du réchauffement planétaire qui pourrait retarder le rétablissement de la couche d’ozone;
à l’arrivée sur le marché de nouvelles substances destructrices de l’ozone;
à la lenteur de la ratification des amendements du Protocole, illustrée à la figure 5(68).
Figure 5

Comme il a déjà été mentionné, les HCFC – les substituts actuels des CFC – devront être éliminés dans les prochaines décennies en raison de leur fort potentiel de réchauffement du globe, de sorte qu’il faudra leur trouver, à eux aussi, des substituts.
Il demeure d’importants stocks d’équipements et de matériels contenant des CFC. L’élimination progressive se poursuit dans les pays industrialisés, qui ont utilisé des CFC depuis leur invention, il y a plus de 50 ans. Si l’on ne parvient pas à éliminer les SACO dans les économies montantes d’Asie, en particulier, le Protocole ne donnera pas les résultats escomptés.
Une grande partie des mousses et matériaux d’isolation contenant des CFC sont dans des décharges, et la libération de ces SACO reste incertaine. En outre, il y a dans le monde un milliard d’appareils de réfrigération et de climatisation, dont un grand nombre sont mal entretenus et présentent des fuites de CFC, et qui sont simplement mis en décharge à la fin de leur vie utile. Ces énormes quantités de CFC finiront sans doute par se retrouver dans l’atmosphère.
En raison de la diminution de la production et de l’utilisation de CFC dans les pays industrialisés et de la poursuite de la production dans les pays en développement jusqu’en 2010, il s’est installé une lucrative contrebande internationale de CFC(69). L’étendue de ce commerce illicite est estimée à 10 p. 100 du commerce légal(70). Au cours des réunions, on a insisté auprès des Parties au Protocole de Montréal pour qu’elles mettent en place des programmes d’octroi de permis et imposent de lourdes sanctions aux contrebandiers. C’est aux États-Unis que ce marché noir des SACO est actuellement le plus important(71). Pour lutter contre ce problème, les pays consultés ont suggéré les mesures suivantes :
rédaction d’une loi;
coordination des travaux des organismes;
mise en place d’un système d’octroi de permis;
formation des procureurs, des agents d’investigation et des agents des douanes(72).
Il a récemment été découvert que, bien que les « gaz à effet de serre » réchauffent l’atmosphère à proximité de la surface de la Terre, ils induisent aussi un refroidissement de la stratosphère qui en modifie l’équilibre radiatif et, donc, renforce le vortex polaire de l’Arctique(73). Il faut savoir que le réchauffement planétaire est lié à l’appauvrissement de l’ozone dans la stratosphère. En février 1999, Hartmut Grassl, directeur du Programme mondial de recherches sur le climat des Nations Unies, a fait de la haute atmosphère sa toute première priorité, pour donner suite aux préoccupations découlant du fait que l’on ne connaît pas assez les changements subis par la haute atmosphère au-dessus des régions polaires habitées de l’hémisphère Nord(74).
La vie sur Terre reste un équilibre délicat entre nombre d’éléments différents. L’utilisation de substances destructrices de l’ozone a mis en péril ce qui constitue l’écran solaire de la Terre. Les effets nocifs de l’augmentation du rayonnement UV-B sont en train d’empirer. Maintenant que les recherches ont confirmé le lien entre le changement climatique et l’appauvrissement de la couche d’ozone, l’échéance de son rétablissement a dû être repoussée(75).
La communauté internationale a fait preuve d’une coopération jamais vue auparavant pour faire face à cette situation. La réduction, le recyclage et le remplacement des SACO progressent. À ce jour, les pays industrialisés en ont réduit la production et la consommation de 85 p. 100(76). De nouvelles technologies sont mises au point pour qu’on puisse éliminer les agents destructeurs de l’ozone. Bien que la concentration de chlore dans la stratosphère soit à la baisse et que l’augmentation des halons ralentisse, plusieurs modèles montrent maintenant que le pic de l’appauvrissement de l’ozone devrait survenir aux alentours de 2020, et non de 2000, comme le suggéraient les estimations précédentes(77). Sans cet effort international pour limiter l’abondance des substances destructrices d’ozone dans l’atmosphère, la situation serait bien pire, et se serait poursuivie pendant de nombreuses décennies de plus.
Si les engagements internationaux sont honorés, la couche d’ozone devrait revenir aux niveaux d’avant 1980 au cours de la seconde moitié de ce siècle(78). Maintenant que l’on connaît mieux la complexité et les interrelations de la chimie et de la mécanique de l’ozone dans la haute atmosphère, il est essentiel que la communauté planétaire respecte pleinement les dispositions du Protocole de Montréal et les efforts de limitation des émissions de gaz à effet de serre pour que l’on puisse espérer rétablir l’équilibre naturel de la production et de la destruction de l’ozone dans la haute atmosphère.
ANNEXE
Substances destructrices de l’ozone
Nom chimique |
Durée de vie, |
PDO |
CFC-11 (CCl3F) |
45 |
1,0 |
CFC-12 (CCl2F2) |
100 |
1,0 |
CFC-113 (C2F3Cl3) |
85 |
0,8 |
CFC-114 (C2F4Cl2) |
300 |
1,0 |
CFC-115 (C2F5Cl) |
1700 |
0,6 |
Halon 1211 (CF2ClBr) |
11 |
3,0 |
Halon 1301 (CF3Br) |
65 |
10,0 |
Halon 2402 (C2F4Br2) |
6,0 |
|
CFC-13 (CF3Cl) |
640 |
1,0 |
CFC-111 (C2FCl5) |
1,0 |
|
CFC-112 (C2F2Cl4) |
1,0 |
|
CFC-111 (C3FCl7) |
1,0 |
|
CFC-112 (C3F2Cl6) |
1,0 |
|
CFC-113 (C3F3Cl5) |
1,0 |
|
CFC-114 (C3F4Cl4) |
1,0 |
|
CFC-115 (C3F5Cl3) |
1,0 |
|
CFC-116 (C3F6Cl2) |
1,0 |
|
CFC-117 (C3F7Cl) |
1,0 |
|
CCl4 Tétrachlorure de carbone |
35 |
1,1 |
Méthyle chloroforme
(C2H3Cl3) |
4,8 |
0,1 |
Bromure de méthyle (CH3Br) |
0,7 |
|
CHFBr2 |
1,0 |
|
HBFC-12B1 (CHF2Br) |
0,74 |
|
CH2FBr |
0,73 |
|
C2HFBr4 |
0,3 – 0,8 |
|
C2HF2Br3 |
0,5 – 1,8 |
|
C2HF3Br2 |
0,4 – 1,6 |
|
C2HF4Br |
0,7 – 1,2 |
|
C2H2FBr3 |
0,1 – 1,1 |
|
C2H2F2Br2 |
0,2 – 1,5 |
|
C2H2F3Br |
0,7 – 1,6 |
|
C2H3FBr2 |
0,1 – 1,7 |
|
C2H3F2Br |
0,2 – 1,1 |
|
C2H4Br |
0,07 – 0,1 |
|
C3HFBr6 |
0,3 – 1,5 |
|
C3HF2Br5 |
0,2 – 1,9 |
|
C3HF3Br4 |
0,3 – 1,8 |
|
C3HF4Br3 |
0,5 – 2,2 |
|
C3HF5Br2 |
0,9 – 2,0 |
|
C3HF6Br |
0,7 – 3,3 |
|
C3H2FBr5 |
0,1 – 1,9 |
|
C3H2F2Br4 |
0,2 – 2,1 |
|
C3H2F3Br3 |
0,2 – 5,6 |
|
C3H2F4Br2 |
0,3 – 7,5 |
|
C3H2F5Br |
0,9 – 1,4 |
|
C3H3FBr4 |
0,08 – 1,9 |
|
C3H3F2Br3 |
0,1 – 3,1 |
|
C3H3F3Br2 |
0,1 – 2,5 |
|
C3H3F4Br |
0,3 – 4,4 |
|
C3H4FBr3 |
0,03 – 0,3 |
|
C3H4F2Br2 |
0,1 – 1,0 |
|
C3H4F3Br |
0,07 – 0,8 |
|
C3H5FBr2 |
0,04 – 0,4 |
|
C3H5F2Br |
0,07 – 0,8 |
|
C3H6FBr |
0,02 – 0,7 |
|
HCFC-12 (CHF2Cl) |
11,8 |
0,055 |
HCFC-123 (C2HF3Cl2) |
1,4 |
0,02 |
HCFC-124 (C2HF4Cl) |
6,1 |
0,022 |
HCFC-141b (C2H3FCl2) |
9,2 |
0,11 |
HCFC-142b (C2H3F2Cl) |
18,5 |
0,065 |
HCFC-225ca (C3HF5Cl2) |
2,1 |
0,025 |
HCFC-225cb (C3HF5Cl2) |
6,2 |
0,033 |
Source : United States Environmental Protection Agency, Global Programs Division, octobre 2000.
Sources originales : Les chiffres figurant dans la colonne Durée de vie sont tirés du tableau 10-8 du document Scientific Assessment of Ozone Depletion, 1998, un rapport du Global Ozone Research and Monitoring Project, de l’Organisation météorologique mondiale. Les chiffres de la colonne PDO sont tirés du tableau 11-1 du document Scientific Assessment of Ozone Depletion. Les espaces en blanc indiquent que cette information ne figurait pas dans la source originale.
(1) National Aeronautics & Space Administration, Ames Research Center, NASA News, avril 2000.
(2) Environnement Canada, L’ozone de l’Arctique : Sensibilité de la couche d’ozone à l’appauvrissement par les substances chimiques et au changement climatique, décembre 1998.
(3) Environnement Canada, Direction générale des sciences atmosphériques et climatiques, L’ozone stratosphérique, janvier 2001.
(4) Paul A. Newman, SAGE III Ozone Loss and Validation Experiment, SOLVE: A NASA DC-8, ER-2 and High Altitude Balloon Mission, National Aeronautics & Space Administration/Goddard Space Flight Center, mars 1999.
(5) Paul J. Crutzen et Veerabhadran Ramanathan, « Pathways of Discovery – The Ascent of Atmospheric Sciences », Science,vol. 290, 13 octobre 2000.
(6) Programme des Nations Unies pour l’environnement (PNUE), Secrétariat de l’ozone, Questions fréquentes sur l’ozone posées au groupe de l’évaluation scientifique, 2000.
(7) Les catalyseurs se caractérisent par le fait qu’ils sont présents dans la même quantité au début et à la fin de la réaction.
(8) Terme général désignant les chlorofluorocarbures (CFC), et d’autres substances de composition similaire contenant du brome.
(9) PNUE, Questions fréquentes sur l’ozone posées au groupe d’évaluation scientifique, 2000.
(10) Thomas G. Chasteen, Ozone’s Problem with Polar Stratospheric Clouds, Département de chimie, Sam Houston State University, printemps 1997.
(11) Particules portant une charge électrique.
(12) Ibid.
(13) Newman, SAGE III Ozone Loss and Validation Experiment, 1999.
(14) Dissociation due au rayonnement ultraviolet.
(15) Richard A. Kerr, « Stratospheric ‘Rocks’ May Bode Ill for Ozone », Science, vol. 291, no 5506, février 2001.
(16) Christiane Voigt et al., « Nitric Acid Trihydrate (NAT) in Polar Stratospheric Clouds », Science,vol. 290, no 5497, octobre 2000.
(18) Environnement Canada, Ozone stratosphérique, janvier 2001.
(19) Environnement Canada, L’ozone de l’Arctique, 1998.
(20) PNUE, State of the Environment Norway, GRID-Adrendal, Original source: UNEP/ (GEMS) library series no 7: The Impact of Ozone Layer Depletion, mai 1997.
(21) Ibid.
(22) Organisation mondiale de la santé, « The Global UV Project Summary », Intersun, octobre 1998.
(23) « 11th MOP to the Montreal Protocol and 5th COP to the Vienna Convention », Linkages, décembre 1999.
(24) PNUE, State of the Environment Norway, 1997.
(25) Organisation mondiale de la santé, « The Global UV Project Summary », 1998.
(26) Environmental Effects of Ozone Depletion: 1991 Update (1991), p. iii.
(27) Synthèse des rapports de l’Ozone Scientific Assessment Panel, de l’Environmental Effects Assessment Panel, du Technology and Economic Assessment Panel, préparée par les présidents des groupes d’évaluation des parties au protocole de Montréal, novembre 1991, p. 6.
(28) Ibid., p. iv.
(29) Crutzen et Ramanathan, « Pathways of Discovery », 2000.
(30) Fred Pearce, « Algal Gloom », New Scientist, août 1998.
(31) Stephen O. Anderson, « Halons and the Stratospheric Ozone Issue », Fire Journal, vol. 8, no 3, mai-juin 1987.
(32) Reinhard Pienitz et Warwick F. Vincent, « Effect of climate change relative to ozone depletion on UV exposure in sub arctic lakes », Nature, p. 404, 484-487, mars 2000.
(34) PNUE, State of the Environment Norway, 1997.
(35) The 2000 ozone hole, British Antarctic Survey, décembre 2000.
(36) PNUE, Questions fréquentes sur l’ozone posées au groupe d’évaluation scientifique, 2000.
(37) Environnement Canada, Initiative pour l’atmosphère moyenne, avril 2000.
(38) Agence spatiale canadienne, SCISAT-1 : Le prochain satellite scientifique canadien, Apogée – Science spatiale, octobre 1999.
(39) Environnement Canada, L’ozone de l’Arctique, 1998.
(40) Fred Pearce, « Chill in the air », New Scientist,mai 1999.
(41) Joyce E. Penner et al.,« Aviation and the Global Atmosphere Summary for Policy Makers », Intergovernmental Panel on Climate Change, United Nations Environment Programme/World Meteorological Organization, avril 1999.
(42) Compte rendu de la 11e réunion des parties signataires du traité de Montréal et 5e conférence des parties signataire du traité de Vienne, Earth Negotiations Bulletin, vol. 19, no 6, décembre 1999.
(43) « Supersonic Aircraft Exhaust Measurements to Help Ozone Aircraft Studies », NASA HQ Public Affairs Office, octobre 1995.
(44) S.A. Montzka, J.H. Butler, J.W. Elkins, T.M. Tompson, A.D. Clarke et L.T. Lock, « Present and future trends in the atmospheric burden of ozone-depleting halogens », Nature, vol. 398, avril 1999.
(45) Environnement Canada, « Modèles à suivre – Trouver des solutions de rechange », La Voie verte, 1997.
(46) Une onde stationnaire est formée de plusieurs ondes identiques superposées.
(47) Région d’amplitude maximale entre deux nœuds voisins d’une onde stationnaire.
(48) « Cooling with Sound: An Effort to Save Ozone Shield », New York Times, 25 février 1992.
(49) Peter T. Landsberg, « Thermodynamics: Cool Sounds », Nature, août 1998.
(50) Mark Alpert, « A Cool Idea », Scientific American, mai 1998.
(51) Naomi Lubick, « Desert Fridge », Scientific American, novembre 2000.
(52) Alan Hall, « What’s the Beef? » Scientific American, novembre 1997.
(53) Ammonia Refrigeration, Occupational Safety & Health Administration, U.S. Department of Labor, mars 2001.
(54) William Murray, « Percées technologiques découlant de l’élimination graduelle des CFC », produit pour le Comité permanent de la Chambre des communes chargé de l’environnement, Direction de la recherche parlementaire, Bibliothèque du Parlement, 6 avril 1992, p. 2.
(55) « Vers des inhalateurs sans CFC – La transition vers des inhalateurs-doseurs dans CFC », La Voie verte, Environnement Canada, juillet 1999.
(56) « No More Ozone-Depleting Solvents », Toronto Star, 16 décembre 1991.
(57) Environnement Canada, « Modèles à suivre », 1997.
(58) Dites aussi « substances appauvrissant la couche d’ozone » (SACO).
(59) Environment News Service, « Stronger Global Ozone Layer Action Agreed », décembre 1999.
(60) Ehsan Masood, « Ozone recovery will be long-term affair », Nature, vol. 373, juin 1998.
(61) Environment News Service, « China Warms to Fridge Project », décembre 1999.
(62) Namrata Singh, « Godrej-GE Appliances to phase out CFC by 2000 », The Financial Express, Inde, avril 1998.
(63) PNUE, Questions fréquentes sur l’ozone posées au groupe d’évaluation scientifique, 2000.
(64) Conseil canadien des ministres de l’environnement, Plan d’action national, Service de la protection de l’environnement, Environnement Canada, janvier 1998.
(65) Environnement Canada, Les impacts sur la santé du rayonnement ultraviolet, septembre 1997.
(66) Autrefois le Service de l’environnement atmosphérique.
(67) Conseil canadien des ministres de l’environnement, Plan d’action national, Service de la protection de l’environnement, Environnement Canada, janvier 1998.
(68) Compte rendu de la 20e réunion du groupe de travail à composition non limitée des parties signataires du traité de Montréal sur les substances nocives à la couche d’ozone : 11-13 juillet 2000, Earth Negotiations Bulletin, vol. 19, no 7, décembre 2000.
(69) David Spurgeon, « Ozone treaty ‘must tackle CFC smuggling’ », Nature, vol. 389, no 219, septembre 1997.
(70) Vinod Chhabra, « Montreal Protocol and After », The Financial Express, Inde, août 1997.
(71) « 11th MOP to the Montreal Protocol and 5th COP to the Vienna Convention », Linkages, décembre 1999.
(72) Ibid.
(73) Drew T. Shindell, David Rind et Patrick Lonergan, « Increased polar stratospheric ozone losses and delayed eventual recovery owing to increasing greenhouse-gas concentrations », Nature, avril 1998.
(74) Pearce, « Chill in the air », 1999.
(75) Peter Aldhous, « Global warming could be bad news for Arctic ozone layer », Nature, vol. 404, avril 2000.
(76) « 11th MOP to the Montreal Protocol and 5th COP to the Vienna Convention », Linkages, décembre 1999.
(77) Shindell, Rind et Lonergan, « Increased polar stratospheric ozone losses and delayed eventual recovery owing to increasing greenhouse-gas concentrations », 1998.
(78) R. Monastersky, « A sign of healing appears in stratosphere », Science News, 18 décembre 1999.